Orvosi azonosítók és vonalkódok olvasásának automatizálása egyedi eszközazonosítási technológiákkal
Contributed By DigiKey's North American Editors
2023-10-26
2013-ban az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) bevezette az egyedi eszközazonosítási rendszert (Unique Device Identification System) vagyis az UDI-szabályt. A szabály célja a betegbiztonság javítása azáltal, hogy a gyártási, forgalmazási és felhasználási pontokon a korszerű dokumentáció segítségével egységes módszert biztosít az orvostechnikai eszközök nyomon követésére és azonosítására. Az európai orvostechnikai eszközökre vonatkozó előírásokhoz vagy más országok hasonló szabályozásaihoz hasonlóan az amerikai UDI-szabály is növeli az adatszolgáltatási pontosságot és megkönnyíti az elemzést visszahívás vagy nemkívánatos esemény esetén.
2023. szeptember 24-től kezdve az FDA kötelezi a gyártókat az egészségügyi eszközökkel kapcsolatos országos tételkód (National Health Related Item Code) és a gyógyszerkód (Drug Code Number) azonosítók jelenlétére az eszközök címkéin és csomagolásán. Az ettől a dátumtól kezdve címkézett valamennyi orvostechnikai terméknek teljes mértékben meg kell felelnie az UDI-előírásoknak. Ezek az előírások a következőkre vonatkoznak:
- a 3. osztályba tartozó, életvédelem szempontjából kritikus termékek, mint például a pacemakerek és a beültetett protézisek;
- a 2. osztályba tartozó, közepesen kritikus termékek, mint például fecskendők, katéterek és felszívódó varratok;
- az 1. osztályba tartozó, alacsonyabb kockázatú termékek, például fogselyem, orvosi köpenyek és oxigénmaszkok.
Az előírások teljes körű érvényesítése azt jelenti, hogy ha egy orvostechnikai eszköz nem rendelkezik szkennelhető vonalkóddal, akkor többé nem minősül érvényes illetve használható terméknek, még akkor sem, ha ember által olvasható címkék vannak rajta, és még akkor sem, ha a termékről általában feltételezhető, hogy a legtöbb felhasználó számára könnyen azonosítható. A rendelkezések e teljes körű érvényesítése ösztönözni fogja az egészségügyi ágazat általi teljes mértékű elfogadást az orvosi biztosítási igények beterjesztésére vonatkozólag is.
 1. ábra: Egyes kézi DPM-kód olvasók (DPM, direct part marking) fejlett világítással és egyéb olyan szoftverekkel rendelkeznek, amelyek automatikusan megtalálják a szimbólumokat, és automatikusan konfigurálják magukat az adott DPM-kód és szubsztrátum olvasásának optimalizálásához. Az itt látható LVS-9585 mind a DPM-alkatrészek, mind a nyomtatott címkék ellenőrzésére képes, átfogó elemzés és jelentéskészítés céljából (kép: Omron Automation)
1. ábra: Egyes kézi DPM-kód olvasók (DPM, direct part marking) fejlett világítással és egyéb olyan szoftverekkel rendelkeznek, amelyek automatikusan megtalálják a szimbólumokat, és automatikusan konfigurálják magukat az adott DPM-kód és szubsztrátum olvasásának optimalizálásához. Az itt látható LVS-9585 mind a DPM-alkatrészek, mind a nyomtatott címkék ellenőrzésére képes, átfogó elemzés és jelentéskészítés céljából (kép: Omron Automation)
A felelősség az ajánlatkérőjé (márkahordozóé)
Az Egyesült Államokban az UDI-kódok pontosságáért és minőségéért minden egyes orvostechnikai termék esetében a szellemi tulajdonos és a terméket forgalomba bocsátó személy felel. Ez különösen fontos, mivel az orvostechnikai termékek piacának nagy része esetén a gyártás más szervezetek létesítményeiben történik, kiszervezett szerződéses formában. Ezért a szerződő fél felelőssége, hogy biztosítsa, hogy a teljes ellátási lánc az UDI-szabálynak megfelelő legyen, biztosítva a pontos címkézést is.
Az egyedi eszközazonosítási technológia eredete
Az UDI-kódok statikus eszközazonosítók. A csomagban lévő tételek mennyiségi változása miatt azonban szükségessé válhat egy új azonosító bevezetése. Ennek módját és formáját a kibocsátó ügynökségek diktálják. Ugyanígy, az eszköz csomagolásakor szükséges sterilitási körülmények megváltoztatása következtében az eszköz azonosítója is módosulhat. Az eszköz rendeltetési piacának (az az ország, ahol az eszközt értékesíteni fogják), a címke nyelvének vagy a CE-jelölésnek a megváltoztatása szintén szükségessé teheti az eszköz azonosítójának megváltoztatását.
Az UDI-szabály előtt az orvostechnikai eszközök gyártói a termékeiket leggyakrabban mindig megjelölték egy alkatrészszámmal. A forgalmazó módosította ezt az alkatrészszámot, majd ezután az egészségügyi szolgáltató vagy a kórház is. Mivel mielőtt egy alkatrész eljutott volna a beteghez minden entitásnak jogában állt megváltoztatni az alkatrészszámot, szinte lehetetlen volt nyomon követni a termékeket, kezelni a visszahívásokat, megakadályozni a hamisítást, vagy pontosan és hatékonyan rendelni új készleteket.
Kapcsolódó tartalom: Robusztus nyomonkövethetőségi megoldások bevezetése
Jelenleg minden eszközhöz egy szabványosított és nem módosítható azonosítót, egy úgynevezett UDI-kódot rendelnek hozzá, hogy minden szervezet számára lehetővé tegyék az eszköz gyorsabb és pontosabb azonosítását, amivel végső soron az orvosi hibák csökkenthetők. Ez az UDI-kód egy alfanumerikus kód, amely két kulcsfontosságú adatot tartalmaz:
- eszközazonosító; és
- gyártási azonosító.
Az eszközazonosító egy adott eszközhöz rendelt statikus címke, amely tartalmazza a címkézőt (általában az eszköz gyártóját) és az eszköz konkrét modellszámát. Ezzel szemben a gyártási azonosító olyan adatokat tartalmaz, amelyek változhatnak, és a benne foglalt adatok nagy része opcionális. Ezek lehetnek tétel- és sorozatkódok, sorozatszámok, lejárati dátumok és gyártási dátumok. Röviden, a választható adatok lehetnek bármik, amit a gyártó vagy a címkéző szükségesnek tart az eszköz nyomon követésének támogatásához.
Minden UDI-címkének tartalmaznia kell ezeket az információkat két formában:
- ember által olvasható forma (egyszerű szöveg); és
- gépi olvasható forma (vonalkód vagy RFID-olvasó általi olvashatóság).
Ha egy eszköz többféle orvosi alkalmazásra is megfelel, az UDI-kódot közvetlenül az eszközön kell feltüntetni, nem pedig a csomagolásán. A szabály a többször használható eszközökre is vonatkozik.
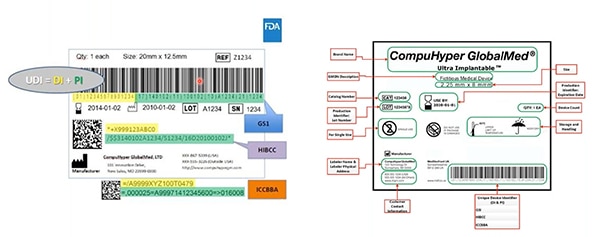 2. ábra: Az UDI-kódot kibocsátó ügynökségek – például a GS1, a HIBCC vagy az ICCBBA – hozzák létre az UDI-kódokat, kijelölik az UDI-kódok megengedett szimbolikáját, meghatározzák, hogy mely technológiák kapcsolódhatnak az UDI-kódokhoz, továbbá meghatározzák az UDI-jelölések előírt minőségét. Ezen a mintán sárgával vannak kiemelve az eszközazonosítók, zölddel pedig a gyártási azonosítók. Az egyéb elemek közé tartoznak az ember által olvasható információk, melyeket kódolt formában a géppel olvasható vonalkód szintén tartalmaz (kép: FDA)
2. ábra: Az UDI-kódot kibocsátó ügynökségek – például a GS1, a HIBCC vagy az ICCBBA – hozzák létre az UDI-kódokat, kijelölik az UDI-kódok megengedett szimbolikáját, meghatározzák, hogy mely technológiák kapcsolódhatnak az UDI-kódokhoz, továbbá meghatározzák az UDI-jelölések előírt minőségét. Ezen a mintán sárgával vannak kiemelve az eszközazonosítók, zölddel pedig a gyártási azonosítók. Az egyéb elemek közé tartoznak az ember által olvasható információk, melyeket kódolt formában a géppel olvasható vonalkód szintén tartalmaz (kép: FDA)
Minden eszközt be kell jegyezni a globális UDI-adatbázisba, hogy visszahívás esetén nyomon követhető legyen, és az adott eszközre vonatkozó információk nyilvánosan hozzáférhetők legyenek. Az eszközgyártók kérésére az FDA által akkreditált kibocsátó ügynökségek egyedi azonosítókat is létrehozhatnak, amelyeket ezután a gyártók elhelyezhetnek a termékeiken.
Kapcsolódó tanulmány: A nyomonkövethetőség aktualizálása
UDI-kód szkennelési technológiák és módszerek
Az UDI-címkék a gyártástól a felhasználásig tartó útjuk során többféleképpen ellenőrizhetők.
Inline ellenőrzés esetén nagyobb gépekbe integrált technológiákról van szó, amelyek nagy mennyiségű terméket dolgoznak fel gyorsan és pontosan a tömeggyártás során. Ezek a fejlett szoftverekre épülő technológiák esetenként ipari minőségű címkenyomtatók formájában jelennek meg. Ezek a nyomtatók képesek saját inline ellenőrzésre, hogy az UDI-információk a címke előállítása után a szigorú ipari szabványoknak megfelelően a címkegyártás helyén azonnal olvashatók legyenek. Például az Omron Automation V275 típusú ellenőrző készülékeit a Zebra hőnyomtatókkal használják az ISO 15426 és a kibocsátó hatóság (GS1) szabványainak való megfeleléshez az FDA-megfelelőség érdekében.
Kapcsolódó tartalom: Nyomonkövethetőségi megoldások az Omrontól
Máshol az inline ellenőrzés az automatizált gyártósorok szállítószalagjait kísérő speciális gépi látórendszerek formájában valósul meg, amelyek a nagy sebességű gyártósori futószalagokon vegyesen található termékeknél vonalkódolvasást végeznek a megfelelő UDI-címkézettségnek rendkívül gyors és pontos ellenőrzéséhez. Az Omron Automation MicroHAWK kínálata a fejlett érzékelőknek a miniatürizált felépítésnek és a kiegészítő Ethernet/IP és PROFINET csatlakozási lehetőségeknek köszönhetően kiemelkedik a többi közül.
Kapcsolódó tartalom: Kerülje el a téves címkézésből eredő felelősségre vonhatóságot
Ezzel szemben az offline UDI-ellenőrzés a minőség biztosítása érdekében a címkék tételes mintavételezésére a legalkalmasabb. Amikor az orvostechnikai eszközök kikerülnek egy létesítményből vagy megérkeznek oda, gyakran alkalmaznak offline ellenőrzést véletlenszerűen kiragadott minták ellenőrzésére, ezzel egészítve ki az online ellenőrző rendszereket a forgalmazási útvonal egy későbbi szakaszában.
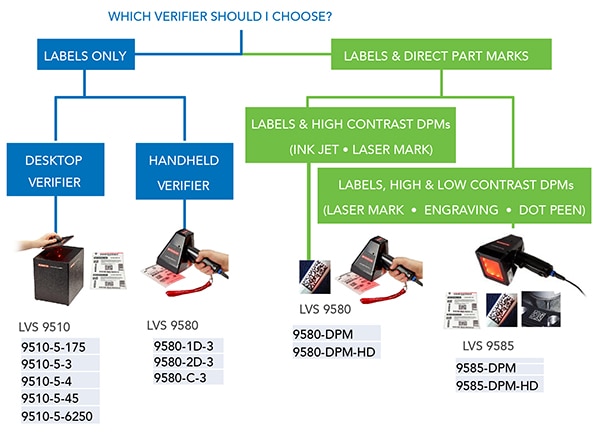 3. ábra: A közvetlenül a termékeken lévő UDI-kódok esetében más típusú ellenőrző készülékeket szükséges alkalmazni, mint a címkékre nyomtatott UDI-jelölések esetében (kép: Omron Automation)
3. ábra: A közvetlenül a termékeken lévő UDI-kódok esetében más típusú ellenőrző készülékeket szükséges alkalmazni, mint a címkékre nyomtatott UDI-jelölések esetében (kép: Omron Automation)
Valójában minden orvosi forgalmazási és egészségügyi tevékenység végzésekor előnyös lehet az ISO-konform hitelesítők használata. Nézzük meg az Omron LVS 95XX sorozatú offline UDI-ellenőrző készülékeit. Ezeket a következő területeken alkalmazzák:
- a kódokat létrehozó lézeres jelölőállomásokon és címkenyomtatókon;
- a kódoknak a termékekre történő felkerülésekor, ami történhet a kódok létrehozási területén kívül, de nem feltétlenül;
- minőségellenőrző állomásokon, a sablonok, formázások és egyéb kódelemek megerősítésekor.
Offline UDI-hitelesítő típusok meghatározása
Egy adott alkalmazáshoz egy legmegfelelőbb offline UDI-hitelesítő készüléket választani számos paramétertől függ.
Vonalkód mérete: A nagyméretű vonalkódokat gyakran könnyebb beolvasni olyan készülékekkel, amelyeknek a lencse gyújtótávolsága és az érzékelő mérete általi fizikai kialakításnak köszönhetően nagy látómezeje van. Vegyük például az Omron Automation LVS-9510 asztali UDI-kódhitelesítőit. Ez a termékcsalád lineáris és 2D címkék olvasására egyaránt alkalmas. Az öt különböző modell mindegyikének más-más a látómezeje, így a tervezők az ellenőrizendő vonalkód méretének megfelelő változatot választhatják. Az összefűzési funkciónak köszönhetően a látómezőnél szélesebb vonalkódok is leolvashatók.
Ezenkívül mindegyik LVS-9510 képes automatikusan meghatározni, hogy a kód kiértékeléséhez mely jelölési rendszert szükséges alkalmazni és beállítani a rekesznyílást, valamint azonosítani és kiemelni a problémás pontokat.
 4. ábra: Az ISO-szabványoknak megfelelő vonalkód-ellenőrzést megkönnyítik a lineáris (1D) és a kétdimenziós (2D) kódok ellenőrzésére egyaránt alkalmas berendezések. Ezek a berendezések némelyike képes automatikusan meghatározni, hogy a kód kiértékeléséhez mely jelölési rendszer alkalmazandó, valamint azonosítják és kiemelik a problémákat. Az itt látható LVS-9510 összefűzési funkcióval is rendelkezik, amely lehetővé teszi a látómezőnél nagyobb vonalkódok osztályozását is (kép: Omron Automation)
4. ábra: Az ISO-szabványoknak megfelelő vonalkód-ellenőrzést megkönnyítik a lineáris (1D) és a kétdimenziós (2D) kódok ellenőrzésére egyaránt alkalmas berendezések. Ezek a berendezések némelyike képes automatikusan meghatározni, hogy a kód kiértékeléséhez mely jelölési rendszer alkalmazandó, valamint azonosítják és kiemelik a problémákat. Az itt látható LVS-9510 összefűzési funkcióval is rendelkezik, amely lehetővé teszi a látómezőnél nagyobb vonalkódok osztályozását is (kép: Omron Automation)
Vonalkód típusa: A szkennereknek a HIBCC, az ICCBBA vagy (2023-tól a leggyakrabban) a GS1 által kiadott vonalkódformátumokat kell olvasniuk. A GS1 határozza meg az UPC-k, a lineáris vonalkódok és a 2D-s adatmátrix-vonalkódok méretét, formátumát és felbontását.
UDI-jelölés helye: Vegyük példaként az orvostechnikai eszközöknél használt közvetlen alkatrészjelölést (DPM). Ezek a jelölések hihetetlenül aprók is lehetnek, különösen, ha azok sebészeti műszereken és beültethető gyógyászati eszközökön találhatók. Az ilyen DPM UDI-jelölések olvasásához és ellenőrzéséhez az Omron LVS-9580 és LVS-9585 ultra-nagy sűrűségű kézi ellenőrző készülékei olyan speciális lencsével rendelkeznek, amellyel számtalan típusú DPM osztályozható, beleértve a 0,05 miliméter alatti cellaméretűeket is. A következetes olvasási pontosság az LVS-9580-ben és az LVS-9585-ben lévő ipari minősítésű lencséknek köszönhetően biztosított. A legkifinomultabb tulajdonságok a szkennerek belsejében található, nagymértékben szabályozható és kalibrálható világítási technológiák. A többféle látómező mellett a világítás a rögzített UDI-képek azonnali optimalizálását is lehetővé teszi. Ez különösen fontos, mivel a kódszabvány nem teszi lehetővé az utólagos korrekciókat vagy képmanipulációkat.
További információk az UDI-szkennerek szoftvereiről
A maximális hatékonysághoz a hitelesítő hardvert támogató UDI-szoftvernek intuitív formában kell bemutatnia a diagnosztikai információkat. Ennek a szoftvernek az ISO szabvány által meghatározott paraméterek szerint kell osztályoznia az UDI-kódokat (elsősorban az olvashatóság megerősítése érdekében), és ideális esetben a fokozatos minőségromlást is nyomon kell követnie a sorozatos UDI-ellenőrzéseken keresztül.
Minden egyes UDI-olvasójához (a hardverhez) az Omron mellékeli az összes szükséges szoftvert is. A szoftvert rendszeresen frissítik, hogy lépést tartson a gyorsan fejlődő szabályozásokkal és az új ágazati jogszabályokkal.
Az Omron szkennereiben lévő szoftver egyik fő funkciója a kódok szintaktikai ellenőrzése. Ez röviden annyit jelent, hogy minden vonal- vagy 2D-kódnak pontosan tartalmaznia kell minden vonatkozó információt, beleértve a termék típusát, tételszámát, mennyiségét, lejárati dátumát, szállítási információkat stb. Az így kapott adatsorokat különleges módon kell formázni, hogy lépést tartsanak a változó követelményekkel, módszerekkel és az orvosi termékek rendeltetési helyeivel.
A szkenner gyártója általi rendszeres szoftverfrissítésekkel biztosított, hogy a végfelhasználók naprakészek maradnak még új kódok megjelenésekor is.
Összegzés
Az Egyesült Államok hadserege egykor az orvosi ipar UDI-rendszeréhez hasonló UID termékkövető rendszer teljes körű bevezetését tűzte ki célul. Ennek célja az volt, hogy visszaszorítsa a katonai létesítményekben elveszett, duplikált és nyilvántartásba nem vett készletekkel járó hatalmas pazarlást, a Raytheon kész fegyvereitől kezdve beleértve mindent, az egyetlen kis cég által valamilyen speciális alkalmazáshoz szállított vezérlőkártyákig. Ma az UID-kódolást vegyesen használják.
Az UDI előírások nem fognak ugyanerre a sorsra jutni.
Az UDI-kódok használatának elfogadtatását illetően a mantra egyszerű: Maga a címke a termék. Ha megvizsgáljuk, egyetlen helytelen címke olyan eseményláncolatot okozhat, ami csak pazarolhatja az egészségügyi személyzet idejét, és az orvostechnikai eszköz kidobásra kerül. Ezért az UDI-kódokat a csomagolás minden szintjén, vagyis magán a darabon, a csomagon, a legyártott sorozaton, a ládán és a raklapon is fel kell tüntetni. A sterilizált orvostechnikai eszközökön a sterilizáló plombák belsejében lévő UDI-jelölések jelenléte különösen fontos, mivel elfogadhatatlan a plomba feltörése az eszköz típusának ellenőrzése céljából.
Mivel az FDA 2023. szeptember 24-től megköveteli az UDI-irányelvek teljes körű betartását, az orvosi termékek ellenőrzésére szolgáló korszerű szkennelési technológiák kiemelkedő fontosságúvá válnak az automatizált gyártók, valamint az általuk kiszolgált gépgyártók és végfelhasználók számára.
Az ilyen szkennerek képesek megfelelni az FDA rendkívül specifikus előírásainak, melyek megkövetelik a rendkívül változatos és különböző laboratóriumi, orvosi és klinikai diagnosztikai berendezéseken található címkék hitelesítését. Offline vonalkód-ellenőrzők, nyomon követhetőség maximalizálása, inline gépi látás és fejlett DPM-olvasók.

Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.






